|
|
|
|
|
伊马替尼耐药的“关键先生”找到了 |
|
研究首次证明CDK1是伊马替尼耐药胃肠间质瘤的进攻弱点 |
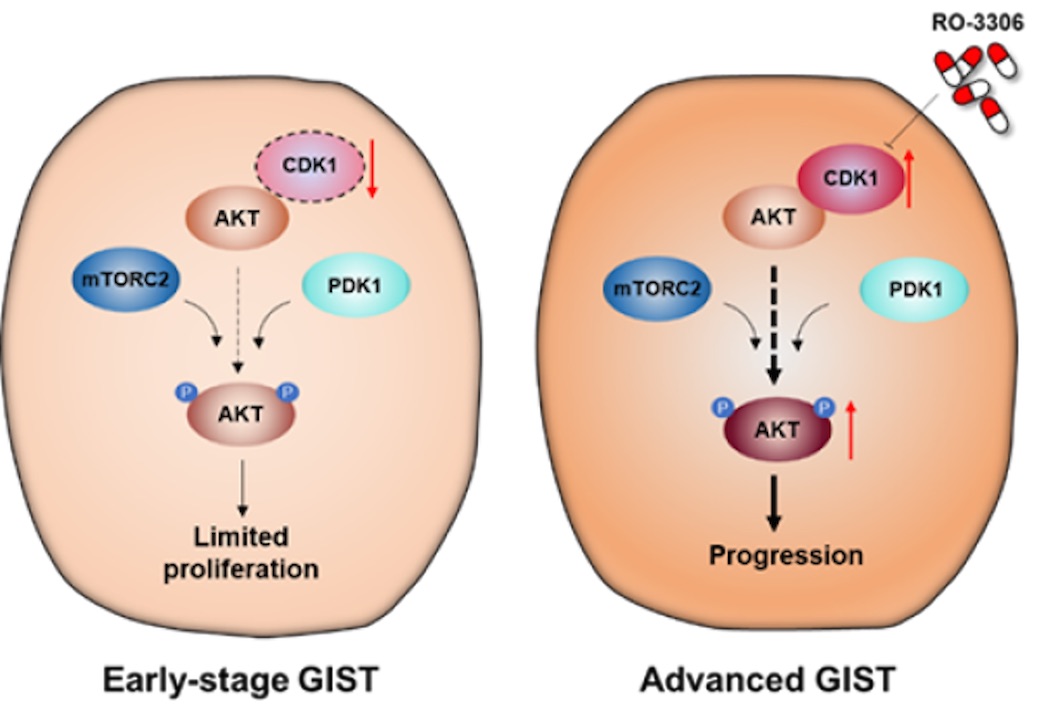
CDK1是伊马替尼耐药胃肠间质瘤(GIST)的进攻弱点。(左)早期GIST中CDK1 不表达,肿瘤细胞的增殖能力有限;(右)晚期GIST中CDK1高表达,激酶CDK1结合其底物AKT并磷酸化473位丝氨酸和308位酪氨酸,从而促进GIST的增殖和进展。
伊马替尼的问世,使胃肠间质瘤(GIST)患者的5年生存率由20年前的15%提高至现在的65%,它也因此迅速成为GIST靶向治疗的“一线明星”。但其成长之路同样遭遇了瓶颈,即几乎所有患者最终都耐药,这也意味着治疗的失败。
虽然伊马替尼耐药后,还有后续的治疗方案,如二线的舒尼替尼和三线的瑞戈非尼等,但治疗效果并不理想,甚至有些副作用明显。“如果不尽快找到伊马替尼耐药胃肠间质瘤的进攻弱点,胃肠间质瘤患者的5年生存率很难突破65%。”中国科学院上海营养与健康研究所研究员王跃祥告诉《中国科学报》。
显然,这项工作很急迫,特别是医生、患者及其家属均期待伊马替尼耐药胃肠间质瘤后的更有效治疗方案。
为此,王跃祥课题组从功能基因组学视角出发,研究首次证明CDK1是伊马替尼耐药胃肠道间质瘤的进攻弱点,并阐明CDK1细胞周期外的新功能及底物,提出CDK1驱动胃肠间质瘤的治疗策略,为克服伊马替尼耐药提供了新的策略及临床前实验数据。研究成果近日发表于《癌症研究》。
伊马替尼耐药之痛
胃肠间质瘤是胃肠道最常见的一种肿瘤,可发生于胃肠道的任何部位,其中60%发生在胃、30%发生在小肠。虽然目前已证实大部分小胃肠间质瘤不会长大,但只要到了晚期,患者对放化疗不敏感,存活率较低。
对于胃肠间质瘤患者来说,2002年是一个特别重要的时间点。这一年,美国食品药品监督管理局(FDA)批准伊马替尼(商品名:格列卫)上市。伊马替尼靶向治疗胃肠间质瘤使患者的预后得到了显著的改善,其所获得的成就与以往相比有了长远的进步,因而成为了肿瘤靶向治疗的标杆。
伊马替尼也被看成“从0到1”的重大突破。据王跃祥介绍,获得美国FDA"重大突破"的认可和走快速审批的“绿色通道”是抗肿瘤药物取得重大突破的两个标志。
伊马替尼问世得益于1998年胃肠间质瘤研究取得的重大进展,即发现胃肠间质瘤的肿瘤细胞起源于胃肠道肌间神经丛周围的Cajal细胞,且高度表达CD117及CD34;进一步研究发现,大多数胃肠间质瘤的肿瘤细胞中的KIT基因存在功能获得性突变,这种突变即为胃肠间质瘤发病过程的关键因素。
《中国科学报》记者了解到,胃肠间质瘤死亡的主要原因是肿瘤复发转移,对于不可切除、转移或复发的晚期胃肠间质瘤患者,国内外治疗指南均推荐伊马替尼作为一线治疗用药。
“伊马替尼还用于术前辅助治疗,缩小肿瘤细胞,以便后续的手术治疗。”王跃祥说。
虽然伊马替尼能给约80%的无法切除或转移的胃肠间质瘤患者提供近3年的肿瘤控制时间,但研究发现,约80%的患者会在2年内出现继发耐药。王跃祥介绍,耐药分为原发耐药和继发耐药。前者是指患者在接受伊马替尼治疗后6个月内出现耐药,占到10%~20%;后者患者接受伊马替尼治疗6个月后出现耐药,约占80%。
“胃肠间质瘤患者一旦发生耐药,容易引起多发耐药,即转移到不同身体部位的肿瘤都会产生耐药。”王跃祥补充道。
当伊马替尼耐药后,常用的靶向治疗药物是二线舒尼替尼、三线瑞卡非尼等以及批准不久的四线治疗方案。然而,伊马替尼耐药后的其他治疗方案并不理想。例如,舒尼替尼是目前伊马替尼一线治疗失败后胃肠间质瘤患者的二线酪氨酸激酶抑制剂药物。有文献指出,与伊马替尼相比,舒尼替尼的不良反应相对较大,如心脏病、难以控制的高血压和甲减症状等。
问题根源还要回到伊马替尼耐药胃肠间质瘤本身上,王跃祥课题组从“源头”出发并开始研究。
有趣的“第2位”
并不是只有王跃祥课题组研究伊马替尼耐药胃肠间质瘤,这一问题是间质瘤基础研究和临床研究领域公认的热点和难题。
“但以往研究倾向于从结构基因组学视角出发,我们换了一个策略,从功能基因组学视角出发。”王跃祥向《中国科学报》表示,前者是以全基因组测序为目标,而后者则是通过识别某个基因在生物模型中的作用来认识新发现基因的功能。
于是,王跃祥课题组根据伊马替尼耐药胃肠间质瘤的发生特征,建立了一系列激酶抑制剂敏感/耐药的胃肠间质瘤模型,通过全基因组系统筛选伊马替尼耐药胃肠间质瘤的潜在进攻弱点。
当筛选到所有必需基因前2位中的第2个时,研究人员非常开心。
“对晚期和早期胃肠间质瘤的多组学测序数据分析,在3个中国胃肠间质瘤队列中发现CDK1在约30%的晚期胃肠间质瘤中高表达,在早期GIST中几乎不表达。”论文第一作者、王跃祥课题组博士生芦晓晶告诉《中国科学报》。
“这项研究工作的不足之处是,只有约30%的晚期胃肠间质瘤,还有70%没找到。”王跃祥承认。因此,该课题组正使用最新方法,以期找出另外70%。
如果排在第2位的CDK1可起到很好的效果,排在第1位基因岂不更重要?
“的确重要。”王跃祥向记者解释道,但这个基因目前没有相应的靶向药物,“暂时先放一放”。
越研究越有趣,王跃祥课题组又对CDK1开展了体内、体外功能实验,进一步证明CDK1高表达的胃肠间质瘤呈现CDK1依赖,敲除CDK1抑制体内体外细胞生长和成瘤,促进细胞凋亡和衰老。
就这样,伊马替尼耐药胃肠间质瘤的“关键先生”被证明是CDK1。

王跃祥和课题组成员观察实验结果。
老蛋白仍有新功能
CDK1蛋白并不是一个新蛋白,往常对其认识是和其他CDK蛋白一样,具有调节细胞周期的功能。但随着研究的不断深入,CDK1FC碰碰胡老虎机法典-提高赢钱机率的下注技巧的细胞周期外的新功能被发现。例如,最近发现CDK1调控表观遗传的调节因子,维持干细胞中特定的表观遗传特征。
王跃祥不否定CDK1调节细胞周期的功能,“但在胃肠间质瘤内,它并不是通过调节细胞周期发生作用的”。
王跃祥课题组进一步研究CDK1,又有了新的发现。
“激酶CDK1直接结合其底物AKT并磷酸化473位丝氨酸和308位酪氨酸,从而促进胃肠间质瘤的增殖和进展。”王跃祥告诉《中国科学报》,该分子机制解释了晚期胃肠间质瘤中AKT高度磷酸化的原因。
虽然敲除CDK1可促进细胞凋亡和衰老,但这并不是目前可行的治疗方法,也不是王跃祥课题组继续研究CDK1的初衷。
于是,该课题组又研究了CDK1的小分子抑制剂RO-3306。研究结果证明,该小分子抑制剂在CDK1高表达的胃肠间质瘤中显著抑制细胞增殖,而对CDK1不表达的胃肠间质瘤细胞则无影响。
“在动物模型中,CDK1抑制剂显著抑制肿瘤生长,证明CDK1抑制剂具有抗伊马替尼耐药胃肠间质瘤的活性。”王跃祥说。而这样的结果为克服伊马替尼耐药提供了新的策略及临床前实验数据。
“在这项研究中,无论是机制研究部分还是功能探索方面,实验设计均很有说服力。”中国医学科学院肿瘤医院深圳医院研究员高静表示,但在精准治疗时代,假如采用CDK1抑制剂开展临床研究,是否可用CDK1表达进行患者筛选以及筛选的标准是什么?伊马替尼耐药前后CDK1表达是否有变化?
这些也是王跃祥课题组需要继续攻关的问题。同时,该课题组也想知道如胃肠间质瘤是怎么形成的、何时会长大进展等一系列科学问题。据悉,王跃祥带领课题组同时在做这项工作。
相关论文信息:https://dor.org/10.1158/0008-5472.CAN-20-3580
版权声明:凡本网注明“来源:中国科学报、科学网、科学新闻杂志”的所有作品,网站转载,请在正文上方注明来源和作者,且不得对内容作实质性改动;微信公众号、头条号等新媒体平台,转载请联系授权。邮箱:
[email protected]。