大脑无疑是身体中最复杂的器官,它能够将各种感觉信息转换为不同的神经信号进而调控运动。这种感觉-运动转换与个体的内部状态密切相关,并受过往经验调节。已有研究表明,社会经验,尤其是性经验,可以引起社会行为相关神经回路的长期改变,并影响社会信息区分、交配、打斗和照顾幼崽等本能行为。然而,关于哪些神经环路编码性经验并影响本能行为抉择并不清楚。在小鼠中,雄性和雌性动物成功交配后通常会失去交配兴趣,即达到性饱足状态。这种内部状态的改变不仅可以避免寻找新伴侣所面临的风险和精力浪费,对提高子代繁殖率也至关重要。然而关于两性大脑中是否存在特异的神经环路编码性饱足状态,以及该编码如何长期影响个体行为抉择并不清楚。
?
2023年2月10日,北京脑科学与类脑研究中心李莹实验室在Science发表题为Hyperexcited limbic neurons represent sexual satiety and reduce mating motivation的研究长文,系统研究了这些问题。该研究首次在小鼠大脑边缘系统的终纹床核中发现可以持续编码过往性经验的神经环路,阐明性经验如何影响两性动物的交配动机,为理解大脑如何编码动机状态并影响本能行为抉择这一重要科学问题提供了新见解。
在针对啮齿类动物的研究中,正常雄性小鼠遇到雌鼠会立即展开嗅探,并在几分钟内开始试图爬跨。如果该雌鼠正处于发情期,她会表现出典型的接受行为(如脊柱前凸),否则会通过坐下或逃离拒绝雄性。成功交配后,雄性和雌性通常会失去交配兴趣,即进入性饱足期。对于有不同经历或处于不同状态的个体,性饱足期可能持续数个小时到数天。
BNSTEsr2神经元在两性动物交配完成后被选择性激活
那么,什么是导致小鼠性饱足的关键因素?研究人员设计雌雄小鼠经历多次插入但在射精前与伴侣分开(没有经历射精)的对照组,发现对照组没有表现出性饱足,这表明射精是驱动两性性饱足状态的关键事件(图1)。
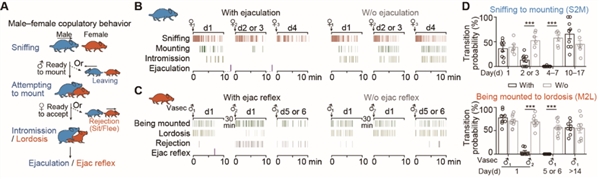
图1. 射精是导致两性动物进入性饱足状态的关键事件
为研究两性小鼠性饱足状态的神经机制,研究人员通过查阅文献发现,在大鼠和长尾鼠中,射精诱导的Fos蛋白表达,存在于犁鼻通路的多个脑区,包括终纹床核(BNST)、中央杏仁核(MeA)和内侧束旁丘脑核(mSPF),但不包括内侧视前区(mPOA)。使用荧光原位杂交(FISH)方法,研究人员发现完成射精的雄鼠与只经历了3-5次插入但没有射精的雄鼠相比,BNST中Fos+神经元数量变化最大。因此,研究人员聚焦在BNST脑区进行深入研究。
过往单核细胞测序(RNA-seq)实验表明,BNST中包含两类具有性别二态性的神经元亚群:BNSTEsr2和BNSTSt18。通过在自由运动的小鼠中进行钙成像发现,大量BNSTEsr2 神经元(>50%)在雄性动物射精以及雌性动物感受到射精时均被强烈激活,而在交配的其他阶段没有明显反应。相反,该区域中另一群表达St18的神经元(BNSTSt18)主要在社交嗅探和其他交配过程中被激活,在射精时没有明显反应 (图2)。
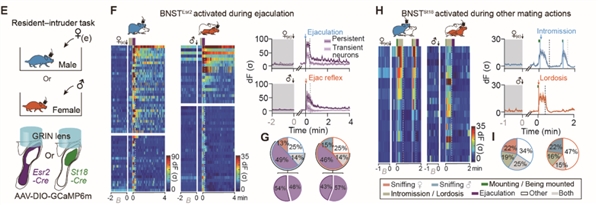
图2. 射精选择性激活两性BNSTpr中表达Esr2的神经元
(A) 部分射精时被激活的BNSTEsr2神经元,在射精结束后仍被持久激活。(B) BNSTSt18神经元在两性中都在射精以外的交配行为中选择性激活。
过度兴奋的BNSTEsr2神经元持续编码两性动物的性饱足状态
雌雄分离后,射精激活的BNSTEsr2神经元反应显著降低,但有一部分神经元在射精结束后30分钟仍保持较强的自发活动,提示这部分神经元可能编码持续性饱足状态。为了进一步检查BNSTEsr2神经元活动是否编码性饱足状态,研究人员将只进行过社会接触、交配但没有性饱足的雄鼠,与交配后达到性饱足的雄鼠独处时的自发放电作比较,发现只有达到性饱足的雄鼠表现出更大幅度和更高频的自发Ca2+活动,并且这种现象可以在整个性饱足期持续数天(图3)。当雄鼠恢复交配能力后,自发Ca2+活动就会恢复到基线水平,并在再次交配且达到性饱足后重新升高。
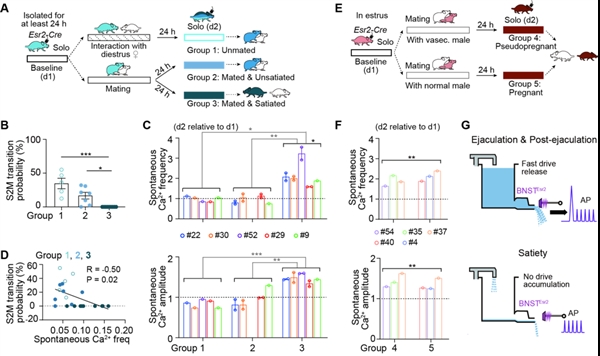
图3. BNSTEsr2神经元活动编码两性动物性饱足状态
与雄鼠一致,雌鼠在交配后24小时BNSTEsr2神经元的自发Ca2+活动也会明显增加,并与是否受孕成功无关。这种增加通常持续整个假孕期、怀孕期和哺乳期,在交配行为恢复后降低到基线水平。
激活雄鼠BNSTEsr2神经元抑制交配动机
研究人员在Esr2-Cre小鼠双侧的BNST中表达抑制性化学遗传病毒hM4Di,并在达到性饱足状态的雄鼠腹膜内注射氯氮平-N-氧化物(CNO)来抑制BNSTEsr2神经元活动。实验发现,七分之六的雄鼠可以在30分钟内恢复其交配行为并成功射精。同样的操作在刚完成交配处于性饱足期的雌鼠中也可以显著恢复其性接受能力(图4)。
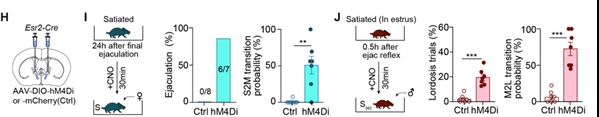
图4. 化学遗传抑制BNSTEsr2神经元活动可以恢复处于性饱足状态的小鼠性行为
为了进一步区分BNSTEsr2神经元是可以抑制交配行为还是交配动机,在雄鼠中,研究人员表达了具有超高光敏感性的视蛋白(SOUL),并在不同的交配阶段进行了经颅光学刺激非侵入性地激活BNSTEsr2神经元。实验发现在嗅探阶段而不是交配开始以后激活BNSTEsr2神经元可以抑制正常雄性小鼠交配起始,这些发现进一步表明BNSTEsr2神经元在抑制交配动机而不是交配动作方面发挥了重要的作用(图5)。
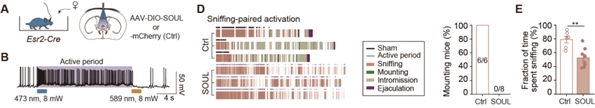
图5. 在早期嗅探期间激活BNSTEsr2神经元抑制雄性小鼠交配动机
BNSTEsr2神经元中HCN离子通道表达上升参与调节雄性小鼠性饱足状态
为了解BNSTEsr2神经活动持续变化的机制,研究人员使用全细胞膜片钳方法,分别在无性经验、性饱足和交配能力恢复的两性小鼠中,记录了BNSTEsr2神经元的电生理特性。在雄性和雌性小鼠中,与无性经验和交配能力恢复的小鼠相比,性饱足(交配后36-48小时)小鼠具有FC碰碰胡老虎机法典-提高赢钱机率的下注技巧BNSTEsr2神经元表现出更高兴奋性。尽管输入电阻和膜电容相当,但在性饱足的BNSTEsr2神经元中,静息膜电位 (RMP) 最高,而rheobases(引发全或无放电所需的最负阶跃电流)最低,提示较小的去极化即可激发动作电位。这种变化在行为恢复的小鼠中大部分恢复,进一步证明了过度兴奋的BNSTEsr2神经元在编码性饱足状态中的作用(图6)。
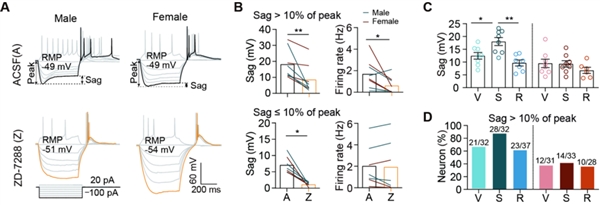
图6. 处于不同状态下BNSTEsr2神经元的Sag电压变化
对已有的BNST单细胞测序结果进行分析,研究人员发现BNSTEsr2神经元中注入负电流显示去极化“下垂”电压,主要由超极化激活的环核苷酸门控 (HCN) 阳离子通道介导。有趣的是,在雄性小鼠中,性饱足小鼠这种“下垂”电压的大小与无性经验或性恢复小鼠的BNSTEsr2神经元相比显著更大,而该现象在雌性小鼠中并不显著。系统重新分析BNST中已发布的snRNA-seq数据集[11],研究人员发现HCN1而不是其他亚基在BNSTp中的Esr2+神经元中相对于其他细胞高度富集。此外,通过FISH方法,研究人员在雄性小鼠的BNSTEsr2神经元中观察到大量HCN1+Esr2+神经元。
使用CRISPR/Cas9技术在BNSTEsr2神经元选择性敲除Hcn1基因,研究人员发现雄性小鼠表现出明显的性饱足状态缺失(图7)。为了进一步测试HCN通道在调节性饱足感中的作用,研究人员在性饱足小鼠颅内两侧BNST给予ZD-7288(HCN抑制剂)或人工脑脊液(载体对照),约1小时后显著恢复了5/6的雄性典型性行为。这些结果表明,在雄性小鼠射精后,HCN通道的激活对于维持性饱足状态是必要的。
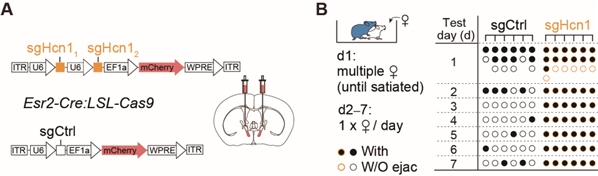
图7. CRISPR/Cas9介导BNSTprEsr2神经元中HCN1敲除后,雄性小鼠能够持续交配
综上所述,该工作在揭示性经验如何引起的大脑内部状态改变这一重要科学问题方面取得了重要突破。这项研究帮助我们理解短暂经验在大脑中持久表征的神经机制,以及这种表征如何长期影响动物行为。此外,该工作还发现短暂性经验可以引起神经元中的离子通道表达的变化,为我们理解性经验如何引起大脑持久改变提供了一个全新的角度 (图8)。
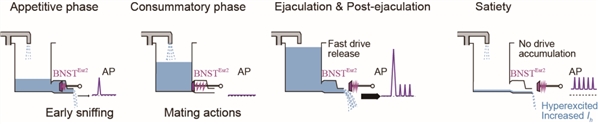
图8. BNSTEsr2神经元参与调控交配动机的机制解释
相关论文信息
该研究工作由北京脑科学与类脑研究中心李莹实验室完成。北京脑科学与类脑研究中心自招博士后周小娟、博士研究生李昂、技术员弭雪为该研究论文的共同第一作者,研究员李莹为通讯作者。
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。