作为生命活动的执行者,蛋白质通过相互作用形成复合物等形式行使其特定的生物学功能。近日,中国科学院大连化学物理研究所研究员张丽华、研究员赵群等研制了一种基于糖苷键的质谱可碎裂型交联剂,显著地提高了交联信息的检索通量和鉴定准确度,同时具有良好的两亲性和生物兼容性,实现了活细胞内蛋白质复合物原位交联和规模化精准解析。相关成果发表在《德国应用化学》上。
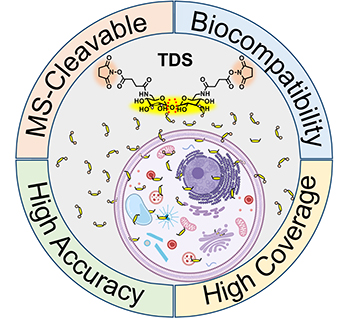
大连化物所供图
细胞内的限域效应、拥挤效应和细胞器微环境等对于维持蛋白质复合物结构和功能至关重要。而化学交联技术,尤其是原位化学交联质谱技术具有规模化分析蛋白复合物原位构象和相互作用界面的优势,已成为活细胞内蛋白质复合物解析的重要技术。但是,目前活细胞原位交联面临着细胞扰动大、交联肽段谱图复杂程度高等问题。因此,如何实现活细胞低扰动下的原位快速交联是蛋白质原位构象和相互作用精准解析的先决条件。
本工作中,团队基于糖分子的高生物兼容性和糖苷键的质谱可碎裂特征,将糖苷键引入到功能交联剂的骨架设计中,筛选并获得了高生物兼容性的海藻糖作为骨架分子,研制了质谱可碎裂型交联剂——海藻糖二琥珀酰亚胺酯。该交联剂较目前已报道的可透膜型化学交联剂,展示了更加优异的细胞活性维持能力,可在低扰动状态下实现细胞内蛋白质复合物的高效交联。
在此基础上,低能量的糖苷键—高能量的肽键的质谱选择性碎裂模式,可以将“工字形”的交联肽段数据分析降幂为常规交联剂片段修饰的线性肽段数据检索,极大地降低了交联肽段谱图分析的复杂性,显著地提高了交联肽段的鉴定效率与准确度。
相关论文信息:https://doi.org/10.1002/anie.202212860
版权声明:凡本网注明“来源:中国科学报、科学网、科学新闻杂志”的所有作品,网站转载,请在正文上方注明来源和作者,且不得对内容作实质性改动;微信公众号、头条号等新媒体平台,转载请联系授权。邮箱:
[email protected]。