近日,长沙理工大学邹振特聘副教授和湖南师范大学杨荣华教授首次报道了一种基于Zn2+配位驱动的RNA纳米组装方法。
该研究以“Zn2+-Coordination-Driven RNA Assembly with Retained Integrity and Biological Functions”为题,于2021年8月17日发表在Angewandte Chemie International Edition上。文章的第一作者是长沙理工大学的邹振特聘副教授和硕士生贺丽蓓,通讯作者是长沙理工大学的卿志和副教授和湖南师范大学的杨荣华教授。
近年来,受自然界中金属配位驱动生物分子交联的启发,各种生物分子(包括DNA、肽、蛋白质和多糖等)作为天然配体已被用于构建生物功能纳米结构。RNA因其具有调控基因表达、生物催化等功能,在疾病治疗中显示出巨大的潜力。例如小干扰RNA(siRNA)、微小RNA(miRNA)和mRNA疫苗等已发展成了药物研发的新星。与DNA类似,RNA中亚胺硝基、磷酸氧基和酮氧基等基团与金属离子具有较强的配位能力,这为RNA的配位自组装和有效递送提供了可能。然而,RNA 分子中的2-羟基可作为内部亲核基团攻击磷中心,导致不稳定环状2,3-磷二酯中间体的形成和RNA水解,导致RNA的稳定性仅为DNA的百万分之一,很多金属离子会催化RNA的水解过程。基于这些事实,RNA作为配体用于功能纳米结构的构建还未被探究。近日,长沙理工大学的邹振特聘副教授和湖南师范大学的杨荣华教授首次报道了一种基于Zn2+配位驱动的RNA纳米组装方法。
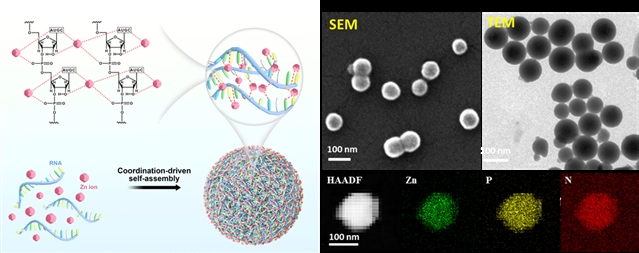
图1:Zn2+配位驱动的RNA纳米组装的示意图及其电镜表征结果
该方法操作简单,只需要将RNA分子和Zn2+在95℃下混合,即可获得具有球形形貌的纳米颗粒(图1)。由于高温消除了RNA复杂的二级结构,因此,该方法适用于不同组成、长度(从20到近1000个核苷酸)和结构的功能性RNA的包载,突显了其普适性。此外,相较于脂质体、阳离子聚合物、无机纳米载体等常用的RNA纳米载体,Zn2+配位驱动组装的RNA纳米颗粒具有优异的RNA包载量和转染效率。更重要的是,凝胶电泳、荧光光谱和ESI质谱等结果表明,包载的RNA保持了其结构的完整性;通过考察合成的绿色荧光蛋白基因mRNA纳米颗粒和抑癌miRNA纳米颗粒的生物学性能,发现Zn2+配位驱动的纳米组装体能够维持包载RNA的生物学功能,发挥高效的荧光信号报告作用(图2)和抗肿瘤作用。

图2:(A-D)Zn2+配位驱动合成的绿色荧光蛋白基因mRNA纳米颗粒(A和C)和环状RNA纳米颗粒(B和D)电镜表征结果;(E-H)绿色荧光蛋白基因mRNA纳米颗粒在HeLa细胞中的转染和表达效果
该工作为RNA配位化学领域的发展提供了新的维度,并且展现了其在RNA药物递送方面的巨大潜力。(来源:科学网)
相关论文信息:https://doi.org/10.1002/anie.202110404