近日,华中师范大学的肖文精教授与陆良秋教授团队在Nature Catalysis上发表了一篇题为“Construction of axial chirality via asymmetric radical trapping by cobalt under visible light”的最新研究成果。
研究团队通过协同的可见光-钴催化策略,首次利用不对称自由基偶联反应实现了外消旋联杂芳基化合物的动态动力学不对称转化。肖文精教授和陆良秋教授为该论文的通讯作者,博士研究生姜烜和熊威为共同第一作者,华中师范大学为第一完成单位。
可见光催化作为一种绿色、可持续的新兴策略,被广泛用于有机合成领域。由于反应往往涉及高活性的自由基中间体,其对映选择性控制仍然存在一定挑战。针对这一难题,有机化学家结合不对称有机催化、过渡金属催化、酶催化(图1a)等立体控制策略发展了有效的不对称可见光催化策略。尽管近几年该领域得到了快速的发展,但主要用于中心手性化合物合成,其它手性骨架的构建目前尚处于起步阶段。2018年,慕尼黑工业大学的Bach教授利用手性双功能光催化剂,首次实现了可见光诱导的外消旋六元内酰胺联烯去消旋化反应(图1b,Nature 2018, 564, 240-243)。之后,其它轴手性骨架的光催化不对称合成鲜有报道。
华中师范大学的肖文精、陆良秋团队长期致力于可见光诱导的不对称催化研究。前期研究中,该研究团队结合可见光催化和钴催化发展了不对称自由基加成反应(Angew. Chem. Int. Ed. 2019, 58, 13375-13379)和芳基卤代物的不对称还原Grignard-type加成(J. Am. Chem. Soc. 2022, 144, 8347-8354)。在本工作中,他们发展了新型的光/钴协同催化策略,实现了外消旋联杂芳基化合物的动态动力学不对称转化。该反应成功的关键在于氧化加成后形成的轴手性芳基钴物种由于吡啶的配位作用,减小了旋转能垒,发生消旋化,随后立体选择性地捕获光催化产生的自由基(图1c)。
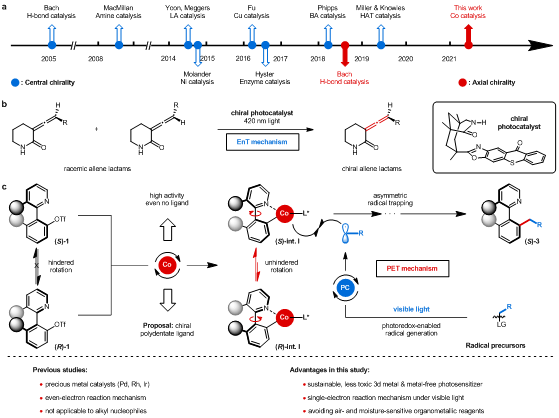
图1:研究背景及反应设计
为验证这一策略的可行性,作者选用外消旋的联杂芳基三氟甲磺酸酯与苄基汉斯酯作为模型反应,对反应条件进行了系统的优化。实验结果表明,由张俊良教授课题组所发展的手性多齿配体L8(Angew. Chem. Int. Ed. 2015, 54, 14853-14857; 本研究所用的这类手性配体由苏州凯若利新材料科技有限公司无偿提供,作者表示特别感谢)对该过程的立体选择性控制和反应效率起到至关重要的作用。在最优条件下,作者对底物范围进行了考察。结果表明,对于不同电性的芳基、杂芳基取代的联杂芳基三氟甲磺酸酯以及汉斯酯底物,该偶联反应都能得到比较好的结果(图2)。此外,对于不对称还原偶联催化体系,该反应对苄基卤代物也有很好的兼容性,普遍以高对映选择性得到一系列含异喹啉骨架的联芳基轴手性产物(图3)。

图2:不对称自由基偶联反应范围(外消旋的联杂芳基三氟甲磺酸酯与苄基汉斯酯)
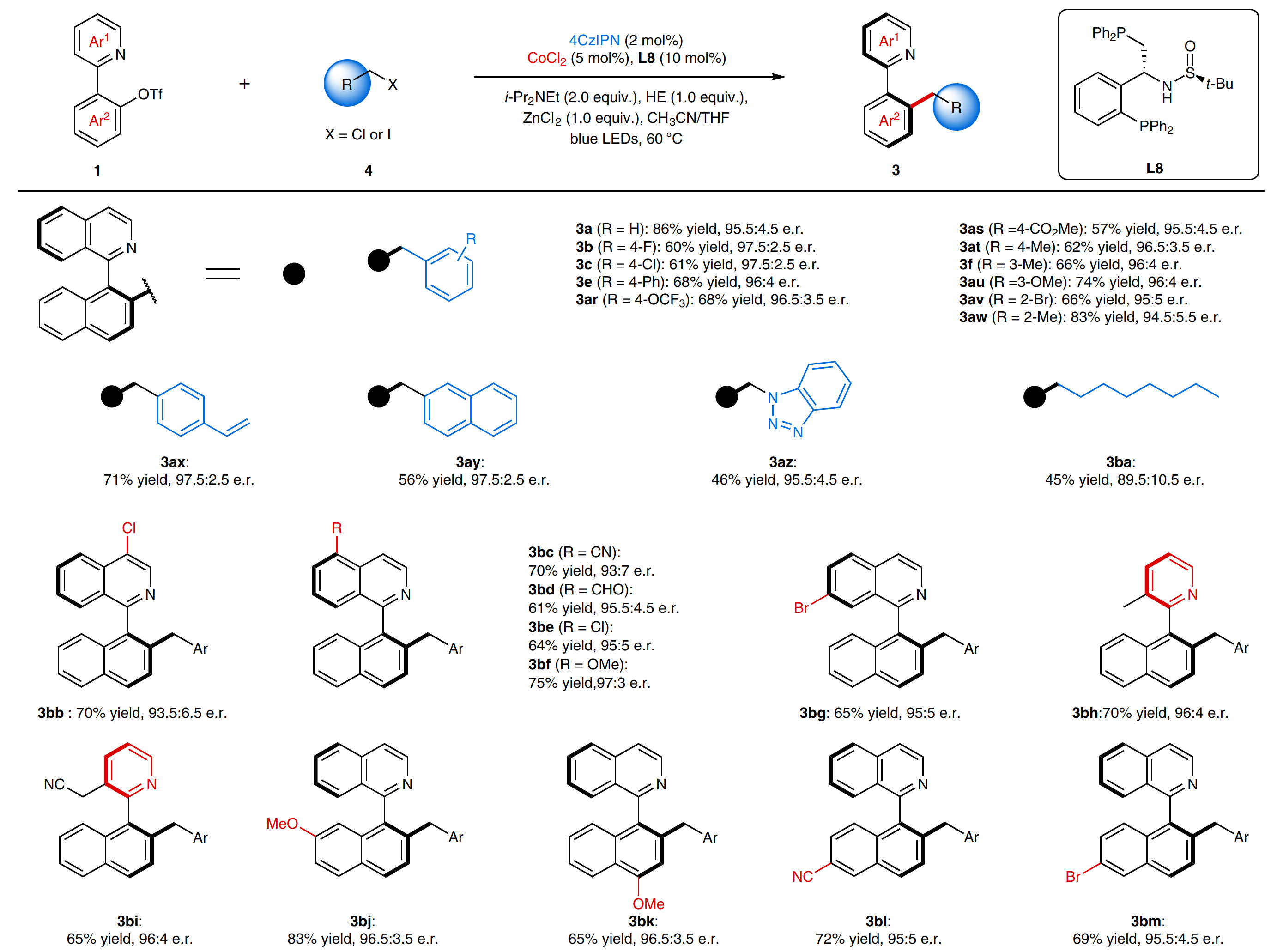
图3:不对称还原交叉偶联范围(外消旋的联杂芳基三氟甲磺酸酯与卤代烷烃)
之后,作者还验证了该方法学的实用性。通过简单的肼解反应,可以得到轴手性伯胺化合物,进而继续以中等到优异的收率合成了一系列双功能的硫脲催化剂和多齿配体。此外,作者发现这类轴手性产物普遍具有聚集诱导发光效应。通过进一步修饰得到的Me-3k具有优异的圆偏振发光性质,其发光不对称因子|glum|为3.02×10-2(测试工作由中科院化学研究所刘鸣华研究员团队帮忙完成,作者表示特别感谢)。与此同时,作者通过与武汉大学的戚笑天教授合作,利用理论计算、控制实验以及高分辨质谱对反应机理开展了深入研究。
综上所述,肖文精/陆良秋团队发展了首例可见光诱导的不对称钴催化自由基偶联反应,实现了外消旋联杂芳基化合物动态动力学不对称转化,以优异的对映选择性制备了一系列轴手性联杂芳基化合物,并研究了相关化合物的光学性质。这项研究不仅为光/钴协同催化不对称自由基偶联反应提供了新的思路,而且还为合成轴手性联杂芳基骨架和相关功能材料提供了新的方法。(来源:科学网)
相关论文信息:https://doi.org/10.1038/s41929-022-00831-1