南方医科大学基础医学院教授白晓春和高学飞团队开发出人软骨类器官高通量药物筛选系统鉴定软骨再生新靶点。相关成果近日发表于《细胞-干细胞》(Cell Stem Cell)。
关节软骨损伤是指由急性创伤或慢性劳损导致的关节软骨破坏,其发病率和患病率均非常高。由于软骨组织缺乏血管、神经分布,且软骨细胞增殖能力较差,因此一旦损伤修复极为困难。目前临床的药物治疗和手术干预均无法修复缺损部位的正常透明软骨。自体软骨细胞是移植治疗软骨缺损的理想细胞来源,但供体细胞来源有限,且体外扩增培养时软骨细胞容易产生去分化。
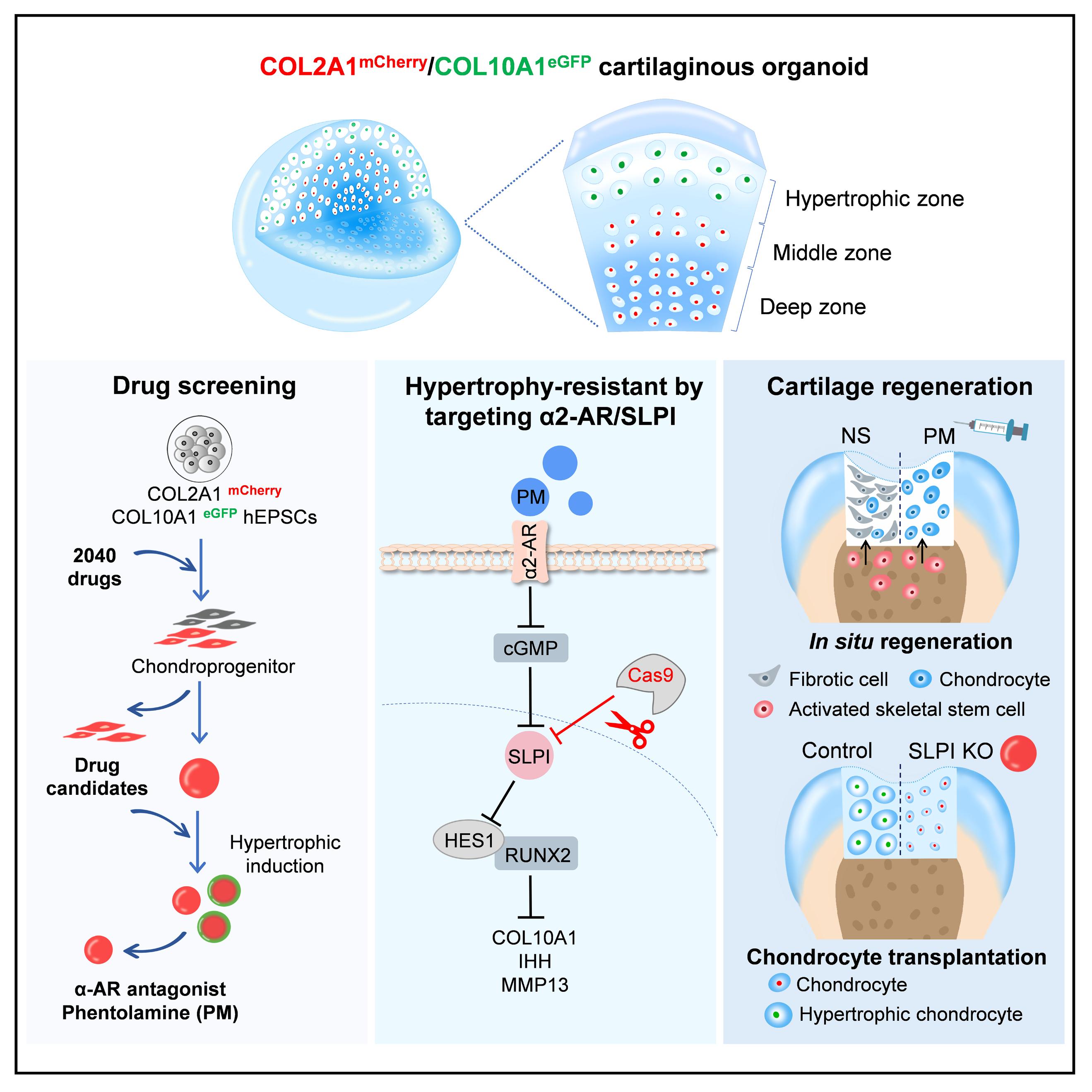
构建软骨类器官并筛选与验证靶向α2-AR/SLPI促进软骨再生的研究模式图。研究团队供图
?
多能干细胞或成体干细胞可通过适当的诱导方式再生软骨,但现有的分化方式及扩增过程中难以完全消除异质细胞,并且容易发生肥大与纤维化的退变倾向。因此,寻找促进软骨再生的治疗靶点,探究软骨细胞表型的维持机制,具有重要的临床应用价值。
研究团队基于人拓展潜能干细胞,利用CRISPR-Cas9基因编辑和干细胞诱导分化技术构建了包含软骨分化标志基因COL2A1-mCherry和软骨肥大标志基因COL10A1-eGFP的双荧光标记软骨类器官;利用该软骨类器官,对两千多种FDA 批准的上市药物进行了高通量筛选,发现α肾上腺素受体抑制剂酚妥拉明具有同时诱导软骨生成和抑制软骨肥大的作用,而α2肾上腺素受体激动剂可乐定和胍法辛具有抑制软骨生成和诱导肥大的作用。
体内实验结果表明,酚妥拉明在小鼠及小型猪软骨缺损模型中可促进内源性干细胞向透明样软骨分化,抑制了纤维软骨形成。在人软骨外植体培养中,酚妥拉明可防止IL-1β诱导的炎性软骨退变。分子机制研究表明,α2肾上腺素受体激活后可以通过cGMP依赖途径产生分泌性白细胞蛋白酶抑制因子(SLPI),SLPI通过上调转录因子RUNX2和增强RUNX2转录活性的HES1,促进COL10A1等肥大相关标志物的表达,从而诱导软骨细胞肥大变性。免疫缺陷小鼠体内移植的SLPI敲除软骨类器官可维持透明软骨细胞表型,并促进关节软骨缺损的修复。
该研究构建的人软骨类器官是一种研究软骨疾病与再生的高效工具,可在体外实时监测软骨形成及肥大过程;利用该工具筛选出的靶向α2肾上腺素受体可有效促进软骨形成并抑制软骨细胞肥大,具有较高的临床转化价值。(来源:中国科学报 朱汉斌)
相关论文信息:https://doi.org/10.1016/j.stem.2024.09.001