2024年7月1日,北京生命科学研究所/清华大学生物医学交叉研究院刘臻实验室与西班牙赫罗纳大学Marc Garcia-Borràs团队合作,在Nature Synthesis期刊发表了题为“Biocatalytic desymmetrization for synthesis of chiral enones using flavoenzymes”的研究论文。该研究分别利用黄素依赖酶的氧化和还原过程实现了立体手性互补的烯酮化合物的合成。具体而言,一方面发展了一种基于黄素依赖酶的不对称脱氢反应体系,通过酶催化的去饱和化过程,高对映选择性地合成含季碳手性中心的环己烯酮类化合物。通过分子动力学模拟以及DFT计算的手段,结合机理实验,作者深入地研究了这一酶催化的反应历程。基于对反应机理的探究,作者随后发现如果利用还原态的黄素酶对环己二烯酮进行不对称还原,则可以获得相反构型的环己烯酮对映体产物。这两种酶催化方法反应条件温和,操作简单,底物适用范围广泛,不管是催化脱氢还是不对称还原反应均可达到优异的底物转化率和高对映选择性。因此,这些方法有望在药物、天然产物等精细化学品的不对称合成中得到应用。该项目的主要内容由刘臻实验室研究生曾清清以及科研助理周谦一完成,其他作者包括研究生代双玉,科研助理赵翔以及西班牙赫罗纳大学的Carla Calvó-Tusell博士。刘臻研究员和Marc Garcia-Borràs研究员为论文通讯作者。
近年来,随着蛋白质工程和生物信息学的飞速发展,功能性蛋白质的开发和应用变得越来越普遍。其中,蛋白酶作为天然的生物催化剂,具有着重要的研究价值和广阔的应用场景。作为合成化学和合成生物学的交叉领域,生物催化研究聚焦于挖掘新颖的酶催化过程,通过高效的酶促方法学解决传统的化学合成难题,同时实现生产成本的降低以及可持续性发展。与传统的小分子催化剂相比,蛋白质催化剂具有可基因编码和调控的特性,可以通过定向进化等手段进行高通量的筛选优化。
该课题关注的烯酮类化合物是合成化学中的重要中间体,可以参与多种经典的化学转化。同时,烯酮类结构在生物活性分子中广泛存在,比如蛋白的共价抑制剂等。大量的文献报道此类分子可作为黄素依赖酶OYE(old yellow enzyme)的底物,发生经典的1,4-还原反应。然而,为了得到烯酮类化合物,传统的化学方法主要依赖于较强的氧化剂或者昂贵的过渡金属催化剂,发展高效的生物催化方法从而制备这类化合物十分必要。

酶催化脱氢反应
由于从环己酮类底物出发直接进行脱氢转化是合成烯酮类化合物最为简洁的合成方案之一,研究人员首先致力于通过酶促不对称脱氢反应来合成目标化合物。尽管自然界中存在不少类型的脱氢酶,然而真正被化学家关注且应用于合成中的例子屈指可数。该研究中,实验人员首先关注到文献记载了一种发现于嗜热菌株中的GkOYE蛋白具有一定的脱氢活性,尽管进一步调研发现相关文献并未成功展示这类酶在手性环己烯酮类化合物合成中的应用前景。
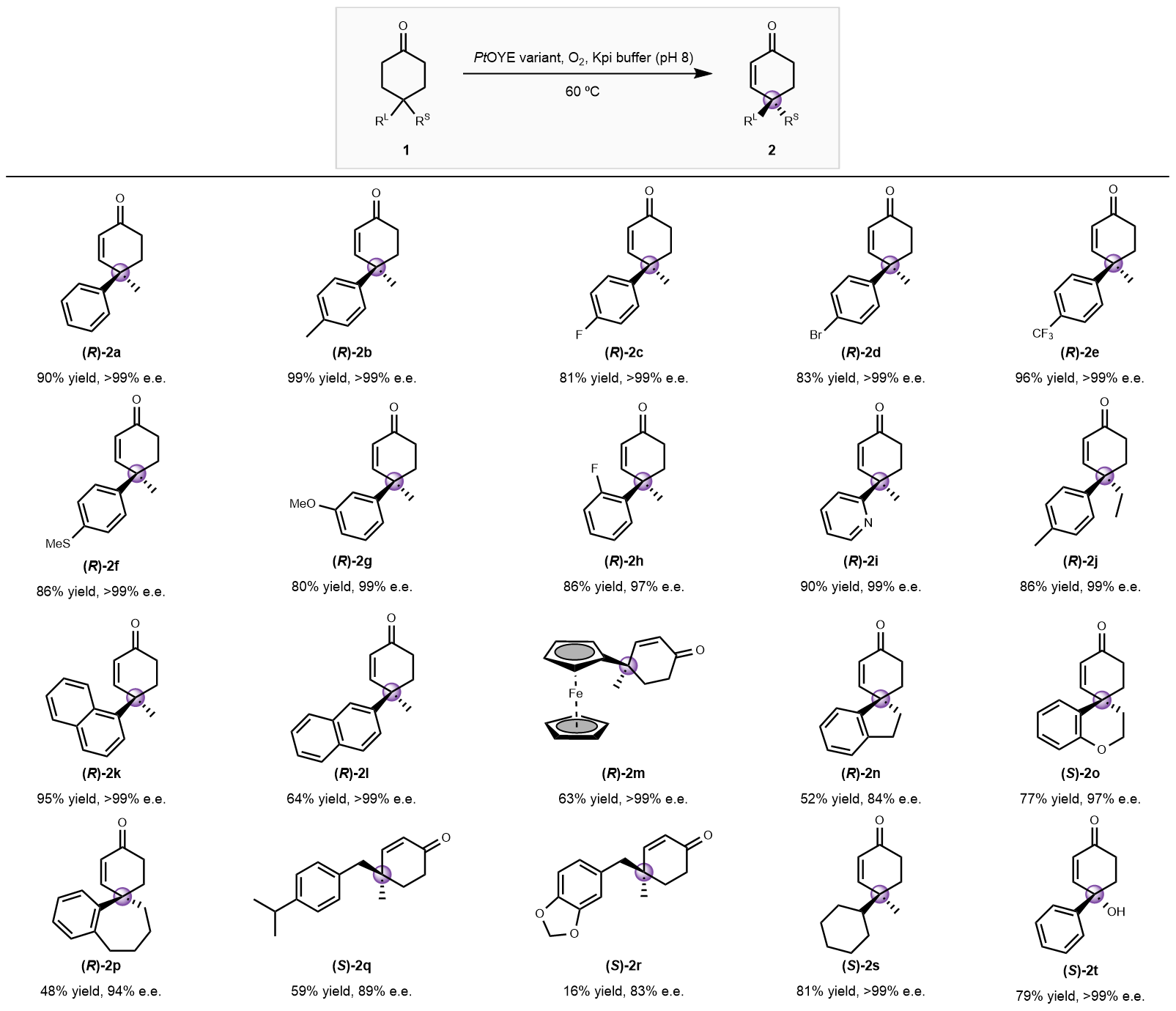
为了探究具有高热稳定性的黄素依赖酶是否可以作为优良的手性催化剂制备环己烯酮,研究人员以GkOYE作为参考序列,使用BLAST工具搜索具有序列相似性的蛋白,最终确定并成功表达了多个文献中尚未研究的热稳定性OYE。后续的筛选实验表明,GkOYE和四种新发现的黄素酶均可以有效地催化底物1a的脱氢反应,并以良好的收率(≥70%)和优异的对映选择性(99% e.e.)得到目标产物2a。其中,来源于Parageobacillus thermantarcticus中的黄素酶(PtOYE)表现出了最高的活性。值得一提的是,这一反应使用的唯一氧化剂为空气中的氧气,因此比现有的化学催化方法更为清洁和温和。
在确定了最优酶催化剂PtOYE和最适反应条件之后,研究人员系统地研究了这一酶促脱氢反应的底物适用范围。实验结果表明,这种生物催化脱氢方法展示出了令人惊讶的底物兼容性和官能团耐受性。具体而言,该方法可以兼容一系列不同电性的官能团,包括苯环上不同取代位置的吸电子或给电子基团,以及杂环、稠环和螺环等复杂结构。值得注意的是,氧化敏感性官能团如硫醚也可被该反应体系兼容,凸显了使用温和氧化剂进行脱氢反应的优势。另外,其他取代模式如4,4-双烷基或4-羟基-4-芳基取代的环己酮也同样适用于这一生物催化体系。最后,研究人员意外发现PtOYE-C26S单位点突变体可以显著提高酶催化效率,体现了这类脱氢酶仍然具有被进一步优化的潜力。
实验人员随后成功将这一酶催化反应放大至毫摩尔级乃至克级规模,并展示了烯酮类化合物的多种下游转化,制备了包括卤代环己烯酮、硅氧双烯和环氧环己酮在内的多种手性合成单元,进一步证明了该酶催化方法的实用性和目标产物的合成价值。
为了探究反应机理,作者通过计算与实验相结合的方式对这一酶促脱氢反应进行了研究。首先,工作人员利用分子动力学模拟(MD simulations)展示了底物与酶分子可能的结合模式。通过计算模拟,作者发现活性空腔中的氨基酸残基H164可以通过与环己酮的羰基形成氢键,参与锚定底物;Y169残基在去质子后可作为关键的碱从环己酮底物的α位攫取质子,使其转化为水相中不稳定的烯醇中间体。该中间体可以在一定程度上被活性口袋附近的极性氨基酸(如H164、H167、K109和Y169)所稳定,随后立体选择性地将β-氢转移至氧化态的FMN辅因子中,从而得到R-构型的环己烯酮产物。DFT能量计算进一步支持了这一机理的合理性。随后,研究人员通过定点突变实验验证了关键氨基酸残基的作用。突变研究结果表明,对H164、H167、K109和Y169等四个氨基酸残基的突变显著降低了酶反应的转化效率。此外,氢氘交换实验支持了Y169作为碱参与形成烯醇中间体的关键作用。
酶催化还原反应
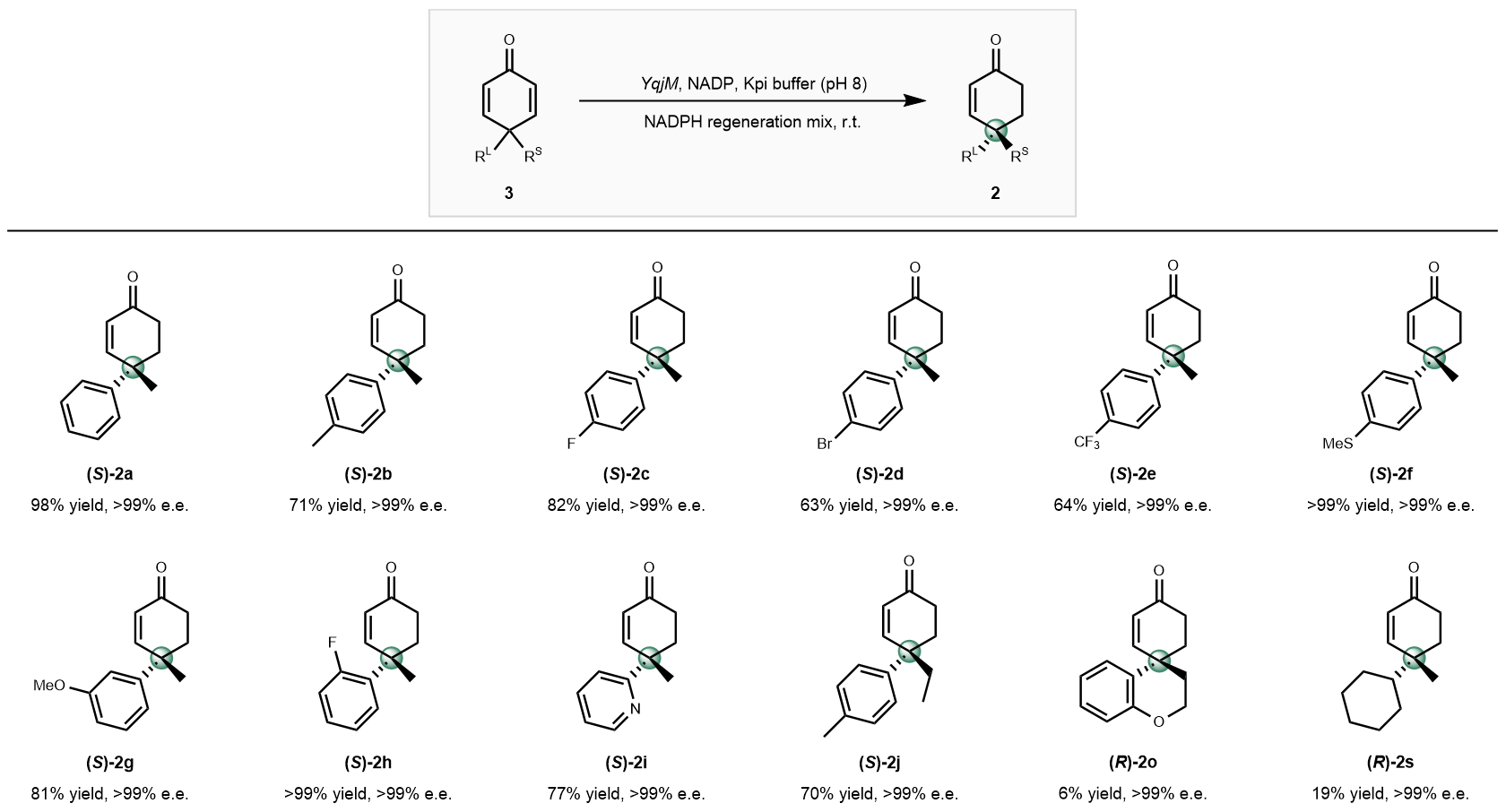
尽管研究人员已成功开发出一种高效的生物催化脱氢系统来获得高立体选择性的烯酮产物,但考虑到两种对映异构体在合成化学中的同等重要性,研究团队希望能够通过酶催化方法进一步获得相反构型的产物。受酶促脱氢机理的启发,研究人员设想如果将环己酮底物替换成环己二烯酮化合物,两者与蛋白酶结合的模式应当相似。由于烯烃还原反应将发生于之前环己酮底物脱氢的同一侧,因此目标产物中环己烯酮的双键位置将与脱氢过程得到的双键位置相反。令人高兴的是,作者的设想在后续的实验中得到了成功的验证。经过对酶催化剂的筛选和反应条件的优化,作者发现YqjM酶可以高效地催化环己二烯酮化合物3a的不对称还原过程(获得98%的产率和 >99%的e.e.)。随后的底物普适性研究进一步表明,这一酶促还原反应同样具有广泛的底物兼容性。
总的来说,利用互补的脱氢与还原转化为获得两种对映异构体的手性烯酮化合物提供了高效且立体选择性的合成方法,凸显了基于黄素依赖酶的去对称化策略在合成化学中的应用价值。这项工作为合成含有手性季碳中心的环己烯酮提供了高效、绿色且立体可控的新策略,在有机合成和药物开发等领域具有重要的应用前景。
该研究得到科技部、清华大学生物医学交叉研究院以及北京生命科学研究所的资助。(来源:科学网)
相关论文信息:https://doi.org/10.1038/s44160-024-00596-4