中国科学院上海药物研究所研究员张继稳团队开发了一种新颖的纳米网格结构载体,包载工程化细胞外囊泡(EVs),可作为肺部给药的潜在治疗平台,用于治疗肺部疾病,尤其是炎症性疾病。12月23日,相关研究发表于《碳水化合物》。
EVs是细胞释放到胞外的纳米囊泡,具有典型的脂质双分子层结构,可保护内容物免受破坏,在细胞通讯间中发挥着关键作用,并参与控制多种生物过程。EVs常被作为天然内源性纳米递送系统用于内源性或外源性药物的递送,但存在循环半衰期短、易脱靶等缺点。
使用干粉吸入剂进行肺部给药可以直接将粉状药物递送到肺部,从而有效提高药物的生物利用度。因此,吸入给药治疗肺部疾病,可以减少对其他器官的毒副作用,是治疗肺部疾病安全有效的方法。
研究人员基于环糊精金属有机骨架的有序结构,采用对称型硼酸酯键交联剂,制备了一种由硼化环糊精框架(BCF)制成的纳米网格载体。纳米网格状结构由数十纳米直径的纳米纤维交织而成,分布有10-300纳米的开放空间,且具有pH/H2O2双响应性。而牛奶来源EVs(mEVs)的粒径为50-150 纳米,处于BCF孔径的主要分布范围内。
短肽序列RGD是一种常见的主动靶向性多肽,对广泛存在于癌细胞和巨噬细胞中的αvβ3整合素有很高的亲和力。研究人员利用一种新型环状RGD修饰mEVs(RGD-mEVs),可以增加mEVs的生物利用度,并进一步优化其稳定性与靶向性。在细胞水平,RGD-mEVs比mEVs有更好的抗炎效果,且BCF 能够捕获并保护RGD-mEV,形成RGD-mEVs@BCF。
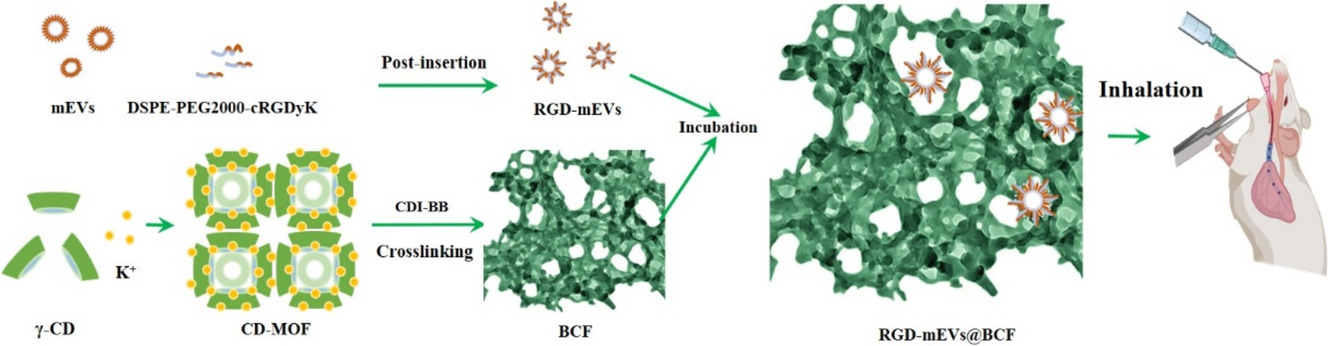 RGD-mEVs@BCF用于肺部递送。图片来源于《碳水化合物》
RGD-mEVs@BCF用于肺部递送。图片来源于《碳水化合物》
?
值得一提的是,RGD-mEVs@BCF具有缓释效果且能响应性释放,在大鼠肺部给药时显示出良好的生物相容性,为基于EVs的给药系统提供了一种新颖设计。
相关论文信息:https://doi.org/10.1016/j.carbpol.2024.123160
版权声明:凡本网注明“来源:中国科学报、科学网、科学新闻杂志”的所有作品,网站转载,请在正文上方注明来源和作者,且不得对内容作实质性改动;微信公众号、头条号等新媒体平台,转载请联系授权。邮箱:
[email protected]。